Substância Pura vs. Mistura: Mitos e Verdades pra Teens de Surabaya!: Diferencie Substancia Pura De Mistura.Dê Exemplo De Cada Uma Delas

Diferencie Substancia Pura De Mistura.Dê Exemplo De Cada Uma Delas – E aí, galera! Já pensou em química como algo maneiro? Tipo, entender a diferença entre uma substância pura e uma mistura pode ser mais fácil do que parece. A gente vai desvendar esse mistério, com exemplos do dia a dia que vocês vão sacar na hora!
Definição de Substância Pura
Substância pura, em resumo, é tipo um time de futebol com jogadores todos iguais. Ou seja, possui apenas um tipo de átomo ou molécula. Isso significa que sua composição é uniforme em toda a sua extensão. Elas têm propriedades características bem definidas, como ponto de fusão e ebulição constantes. Se você aquecer água pura, por exemplo, ela vai começar a ferver sempre na mesma temperatura (100°C ao nível do mar).
Já pensou em água que ferve a 90°C ou 110°C? Isso não é água pura, com certeza!
Temos dois tipos principais: substâncias puras simples (formadas por um único tipo de átomo, como o oxigênio) e substâncias puras compostas (formadas por dois ou mais tipos de átomos ligados quimicamente, como a água).
| Nome | Fórmula Química | Estado Físico (T. Ambiente) | Exemplo |
|---|---|---|---|
| Oxigênio | O₂ | Gasoso | O ar que respiramos (embora seja uma mistura, o oxigênio em si é uma substância pura) |
| Ferro | Fe | Sólido | Uma barra de ferro pura |
| Água | H₂O | Líquido | Água destilada |
| Glicose | C₆H₁₂O₆ | Sólido | Açúcar puro |
Definição de Mistura
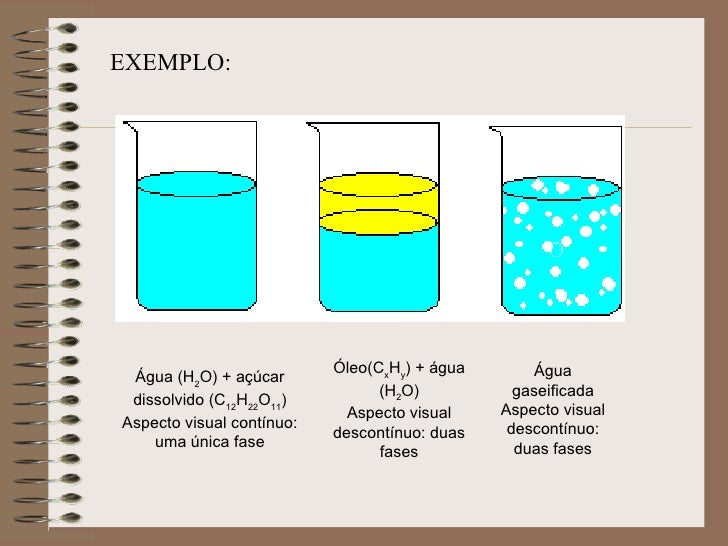
Agora, imagine um time de futebol com jogadores de diferentes times, habilidades e posições. Isso é uma mistura! Misturas são combinações de duas ou mais substâncias puras, que não estão quimicamente ligadas. Elas podem ser homogêneas (com aparência uniforme, como o ar) ou heterogêneas (com componentes visíveis, como areia na água).
As propriedades de uma mistura variam de acordo com a proporção de seus componentes, ao contrário das substâncias puras. Uma mistura de sal e água, por exemplo, terá um ponto de ebulição diferente do da água pura.
- Métodos de separação de misturas: A gente pode separar os componentes das misturas usando diferentes técnicas, como filtração (areia e água), destilação (água e álcool), decantação (óleo e água), evaporação (sal e água), cristalização (sal em solução aquosa), e cromatografia (separação de pigmentos).
Exemplos de Substâncias Puras
Vamos dar uma olhada em alguns exemplos de substâncias puras, seus estados físicos e propriedades:
- Água (H₂O): Líquido à temperatura ambiente, incolor, inodora, sem sabor (pura), ponto de fusão 0°C e ponto de ebulição 100°C (ao nível do mar).
- Oxigênio (O₂): Gasoso à temperatura ambiente, incolor, inodoro, essencial para a respiração.
- Ferro (Fe): Sólido à temperatura ambiente, cinza prateado, maleável, dúctil, bom condutor de eletricidade e calor.
- Açúcar (Sacarose – C₁₂H₂₂O₁₁): Sólido à temperatura ambiente, cristalino, branco, doce.
- Sal de cozinha (Cloreto de Sódio – NaCl): Sólido à temperatura ambiente, cristalino, branco, salgado.
Comparando água e ferro, vemos que são bem diferentes: a água é um líquido a temperatura ambiente, enquanto o ferro é um sólido. A água é um composto, enquanto o ferro é um elemento. Mas ambos são substâncias puras.
Exemplos de Misturas, Diferencie Substancia Pura De Mistura.Dê Exemplo De Cada Uma Delas
Agora, vamos ver alguns exemplos de misturas, classificando-as e explicando como separá-las:
- Ar atmosférico (Homogênea): Mistura de gases como nitrogênio, oxigênio, argônio, etc. Difícil de separar completamente, mas pode-se separar os componentes por liquefação fracionada.
- Água do mar (Homogênea): Água com sais dissolvidos. Pode ser separado por evaporação, deixando o sal.
- Areia e água (Heterogênea): Pode ser separada por filtração.
- Leite (Homogênea): Mistura de água, gordura, proteínas e açúcares. Pode ser separada por centrifugação (separando a nata do resto).
- Salada de frutas (Heterogênea): Mistura de diferentes frutas. Componentes separados manualmente.
Exemplo: Água com açúcar. Se você dissolver bem o açúcar na água, a mistura parece uniforme a olho nu. Isso indica que é uma mistura homogênea. Se você conseguir ver os grãos de açúcar, é uma mistura heterogênea.
Comparando a água do mar e a salada de frutas, vemos que a água do mar é uma mistura homogênea, enquanto a salada de frutas é heterogênea. A composição afeta as propriedades: a água do mar é líquida e salgada, enquanto a salada de frutas tem textura e sabores variados.
Diferenças entre Substância Pura e Mistura: Uma Comparação Detalhada
Vamos resumir as principais diferenças em uma tabela:
| Característica | Substância Pura | Mistura |
|---|---|---|
| Composição | Um único tipo de átomo ou molécula | Dois ou mais tipos de átomos ou moléculas |
| Propriedades | Pontos de fusão e ebulição constantes | Pontos de fusão e ebulição variáveis |
| Métodos de Separação | Não podem ser separados por métodos físicos | Podem ser separados por métodos físicos |
Identificar se uma amostra é pura ou uma mistura depende da observação de suas propriedades e da tentativa de separação dos seus componentes. Na indústria, por exemplo, a pureza dos materiais é crucial para garantir a qualidade dos produtos. Em um laboratório, a pureza dos reagentes é essencial para a precisão dos experimentos.
Como identificar se uma substância é pura através de sua curva de aquecimento?
Uma substância pura apresenta um patamar na curva de aquecimento durante a mudança de estado físico (fusão ou ebulição), indicando que a temperatura permanece constante enquanto a substância muda de fase. Misturas, por outro lado, geralmente apresentam uma variação gradual de temperatura durante a mudança de estado.
Quais são os métodos de separação de misturas mais utilizados na indústria?
A indústria utiliza diversos métodos, dependendo da mistura. Destilação (para separar líquidos com diferentes pontos de ebulição), filtração (para separar sólidos de líquidos), decantação (para separar líquidos imiscíveis), cristalização (para separar sólidos dissolvidos em líquidos) e cromatografia (para separar componentes de misturas complexas) são alguns exemplos.
Existe alguma substância pura que seja encontrada naturalmente na forma 100% pura?
Na prática, encontrar substâncias 100% puras na natureza é extremamente raro. A maioria das substâncias encontradas naturalmente apresenta algum grau de impureza, mesmo que em pequenas quantidades.

